近日,山东大学齐鲁医院神经外科陈安静研究员团队在Chemical Engineering Journal(中科院1区Top,IF=13.2)发表研究“EngineeredEscherichia coliNissle 1917 carrying D-lactate dehydrogenase suppresses glioblastoma malignancy via gut-brain axis reprogramming”,首次揭示D-乳酸作为胶质母细胞瘤(GBM)关键代谢物的致病作用,并构建了表达D-乳酸脱氢酶(LDHD) 的工程化益生菌大肠杆菌Nissle 1917(EcN),通过口服脂质包被的工程菌(Lipo‑EcN‑LDHD) 高效清除体内D-乳酸,重塑肠‑脑轴代谢微环境,显著抑制GBM生长并延长生存期,为GBM的代谢干预治疗提供了全新策略。陈安静为论文独立通讯作者,山东大学齐鲁医院博士后曹群和硕士研究生王甲正为共同第一作者,山东大学齐鲁医院为第一作者和通讯作者单位。
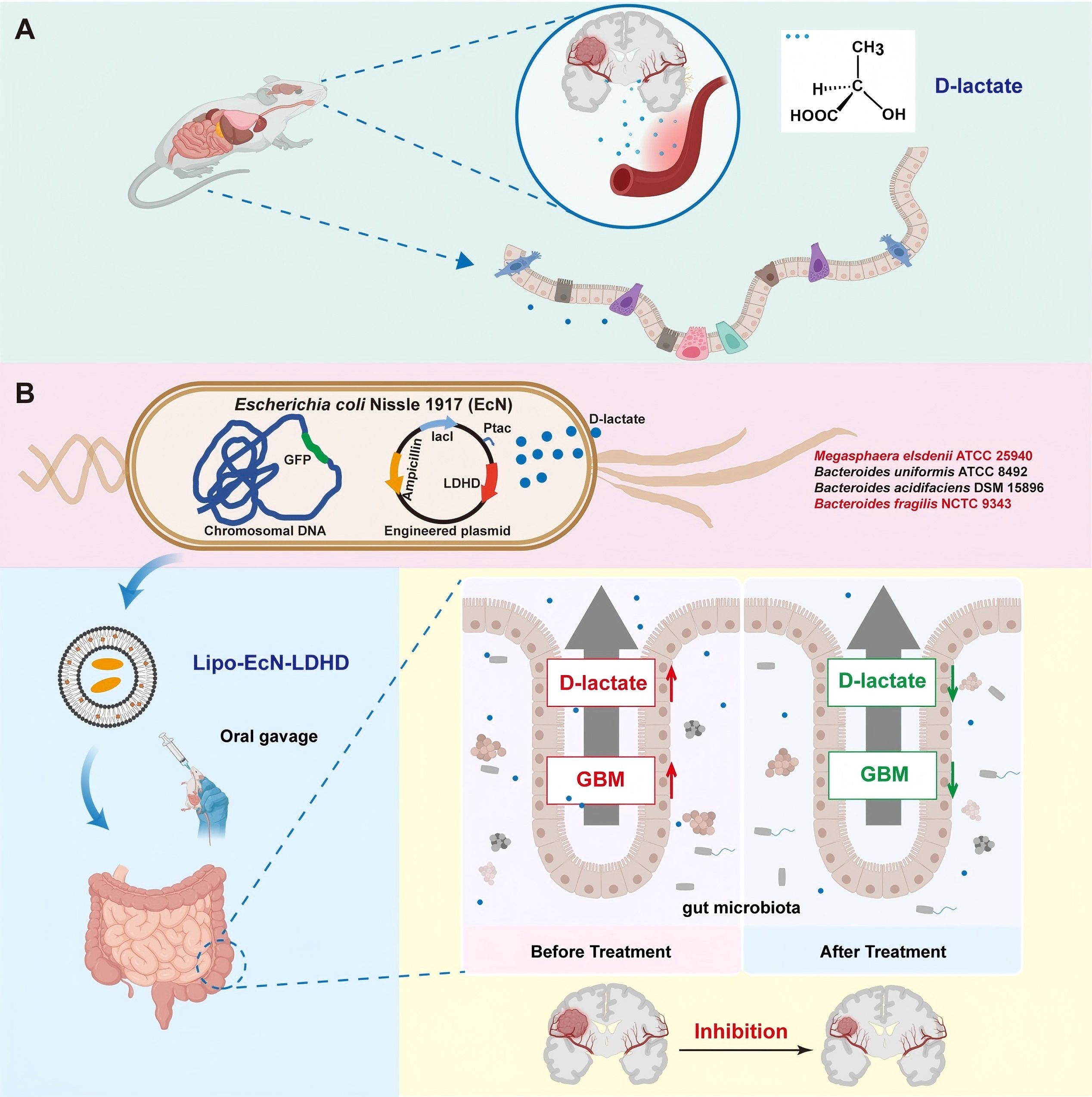
胶质母细胞瘤(GBM)具有高度恶性和免疫抑制的肿瘤微环境,代谢重编程是其核心特征之一。尽管L-乳酸研究广泛,但其对映异构体D-乳酸在GBM中的作用长期被忽视。研究团队通过非靶向代谢组学及体内外模型证实,GBM细胞和荷瘤小鼠血清中D-乳酸水平显著升高,并导致肠道屏障损伤及菌群失调。进一步从人和小鼠肠道菌群中筛选出四株高效代谢D-乳酸的细菌,其中埃式巨球型菌(Megasphaera elsdenii) 活性最强,并从中克隆表达了六种高活性D-乳酸脱氢酶(LDHD)。通过将优选LDHD基因导入益生菌EcN,并经脂质膜包被构建Lipo‑EcN‑LDHD,口服灌胃后可稳定定植于肠道,显著降低血清D-乳酸水平,抑制原位GBM模型中的肿瘤生长,延长荷瘤小鼠总生存期。组织学和免疫组化显示,治疗组肿瘤细胞增殖显著受抑,肠道菌群结构恢复,有害菌减少、有益菌增多。分子对接和点突变证实,精氨酸残基是LDHD催化活性的关键位点。
该研究首次将D-乳酸确立为GBM的可靶向代谢节点,利用合成生物学手段构建了口服工程益生菌平台,实现了“肠道愈脑”的非侵入性代谢干预,为GBM治疗提供了全新的菌群‑代谢‑脑轴策略,并具备良好的临床转化潜力。
在山东大学齐鲁医院神经外科、山东大学脑与类脑科学研究院、山东省脑健康与功能重构重点实验室等平台支持下,陈安静研究员课题组聚焦神经肿瘤基础与转化研究,先后获国家自然科学基金、山东省优青、泰山学者工程等资助,系列成果发表于Clin Cancer Res、Autophagy、Theranostics等期刊。本研究还获得国家自然科学基金、山东省科技厅项目、中国博士后科学基金、山东省博士后科学基金及济南微生态生物医学省实验室项目等资助。
文章链接:https://www.sciencedirect.com/science/article/pii/S1385894726037071